| BLOQUE TEMÁTICO: | Bloque IV. Manifestaciones de la estructura interna de la materia |
|||
| TEMA: | Explicación de los fenómenos eléctricos: el modelo atómico | |||
| SUBTEMAS: | • Características básicas del modelo atómico: núcleo con protones y neutrones, y electrones en órbitas. Carga eléctrica del electrón. | |||
| APRENDIZAJES ESPERADOS | • Describe la constitución básica del átomo y las características de sus componentes con el fin de explicar algunos efectos de las interacciones electrostáticas en actividades experimentales y/o en situaciones cotidianas. | |||
Características básicas del modelo atómico: núcleo con protones y neutrones y electrones en órbita.
Un modelo atómico es una representación estructural de un átomo, que trata de explicar su comportamiento y propiedades. De ninguna manera debe ser interpretado como un dibujo de un átomo, sino más bien como el diagrama conceptual de su funcionamiento. A lo largo del tiempo existieron varios modelos atómicos y algunos más elaborados que otros.
Protón: es una partícula subatómica con una carga eléctrica de una unidad fundamental positiva (+).
Neutrón es una partícula subatómica, un nucleón, sin carga neta.
Electrones en órbita: Tienen carga negativa en cada órbita solo cabe un numero preestablecido de electrones.
La carga eléctrica del electrón es negativa y se representa así: e−
Protón: es una partícula subatómica con una carga eléctrica de una unidad fundamental positiva (+).
Neutrón es una partícula subatómica, un nucleón, sin carga neta.
Electrones en órbita: Tienen carga negativa en cada órbita solo cabe un numero preestablecido de electrones.
La carga eléctrica del electrón es negativa y se representa así: e−
Desde la Antigüedad, el ser humano se ha cuestionado de qué estaba hecha la materia.
Unos 400 años antes de Cristo, el filósofo griego Demócrito consideró que la materia estaba constituida por pequeñísimas partículas que no podían ser divididas en otras más pequeñas. Por ello, llamó a estas partículas átomos, que en griego quiere decir "indivisible". Demócrito atribuyó a los átomos las cualidades de ser eternos, inmutables e indivisibles.
Sin embargo las ideas de Demócrito sobre la materia no fueron aceptadas por los filósofos de su época y hubieron de transcurrir cerca de 2200 años para que la idea de los átomos fuera tomada de nuevo en consideración.
| ||||||||||||||||||||||||||||||||||||||||||||
Descripción de los Modelos Atómicos.
Teoría atómica de Dalton
|
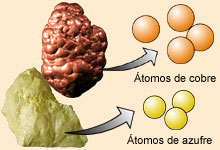 | En 1808, Dalton publicó sus ideas sobre el modelo atómico de la materia las cuales han servido de base a la química moderna. Los principios fundamentales de esta teoría son: 1. La materia está formada por minúsculas partículas indivisibles llamadas átomos. 2. Hay distintas clases de átomos que se distinguen por su masa y sus propiedades. Todos los átomos de un elemento poseen las mismas propiedades químicas. Los átomos de elementos distintos tienen propiedades diferentes. |
3. Los compuestos se forman al combinarse los átomos de dos o más elementos en proporciones fijas y sencillas. De modo que en un compuesto los de átomos de cada tipo están en una relación de números enteros o fracciones sencillas.
4. En las reacciones químicas, los átomos se intercambian de una a otra sustancia, pero ningún átomo de un elemento desaparece ni se transforma en un átomo de otro elemento. | 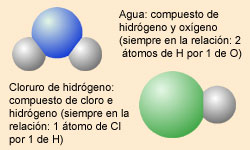 |
Modelo atómico de Thomson
|
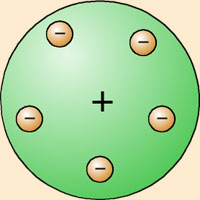 | La identificación por J.J. Thomson de unas partículas subatómicas cargadas negativamente, los electrones, a través del estudio de los rayos catódicos, y su posterior caracterización, le llevaron a proponer un modelo de átomo que explicara dichos resultados experimentales. Se trata del modelo conocido informalmente como elpudín de ciruelas, según el cual los electrones eran como 'ciruelas' negativas incrustadas en un 'pudín' de materia positiva. |
Modelo atómico de Rutherford
|
Rutherford, basándose en los resultados obtenidos en sus experimentos de bombardeo de láminas delgadas de metales, estableció el llamado modelo atómico de Rutherford o modelo atómico nuclear. El átomo está formado por dos partes: núcleo y corteza. El núcleo es la parte central, de tamaño muy pequeño, donde se encuentra toda la carga positiva y, prácticamente, toda la masa del átomo. Esta carga positiva del núcleo, en la experiencia de la lámina de oro, es la responsable de la desviación de las partículas alfa (también con carga positiva). La corteza es casi un espacio vacío, inmenso en relación con las dimensiones del núcleo. Eso explica que la mayor parte de las partículas alfa atraviesan la lámina de oro sin desviarse. Aquí se encuentran los electrones con masa muy pequeña y carga negativa. Como en un diminuto sistema solar, los electrones giran alrededor del núcleo, igual que los planetas alrededor del Sol. Los electrones están ligados al núcleo por la atracción eléctrica entre cargas de signo contrario. |
Modelo atómico de Bohr
|
En 1913 Bohr publicó una explicación teórica para el espectro atómico del hidrógeno. Basándose en las ideas previas de Max Plank, que en 1900 había elaborado una teoría sobre la discontinuidad de la energía (Teoría de los cuantos), Bohr supuso que el átomo solo puede tener ciertos niveles de energía definidos. Bohr establece así, que los electrones solo pueden girar en ciertas órbitas de radios determinados. Estas órbitas sonestacionarias, en ellas el electrón no emite energía: la energía cinética del electrón equilibra exactamente la atracción electrostática entre las cargas opuestas de núcleo y electrón. El electrón solo puede tomar así los valores de energía correspondientes a esas órbitas. Los saltos de los electrones desde niveles de mayor energía a otros de menor energía o viceversa suponen, respectivamente, una emisión o una absorción de energía electromagnética (fotones de luz). |
Sin embargo el modelo atómico de Bohr también tuvo que ser abandonado al no poder explicar los espectros de átomos más complejos. La idea de que los electrones se mueven alrededor del núcleo en órbitas definidas tuvo que ser desechada. Las nuevas ideas sobre el átomo están basadas en lamecánica cuántica, que el propio Bohr contribuyó a desarrollar.
|
Resistencia eléctrica a la mayor o menor oposición que tienen los electrones para desplazarse a
través de un conductor. La unidad de resistencia en el sistema internacional es el ohm, que se representa con la letra griega omega (Ω), en honor al físico alemán George Ohm, quien descubrió el principio que ahora lleva su nombre.
Conductores son los que dejan traspasar a través de ellos la electricidad.
Entre éstos tenemos a los metales como el cobre.
En general, los metales son conductores de la electricidad.
 |
Aisladores o malos conductores, son los que no permiten el paso de la corriente eléctrica, ejemplo: madera, plástico, etc.
Te dejo un link sobre el descubrimiento del electrón:
http://www.hiru.com/fisica/el-descubrimiento-del-electron
y este video para que reafirmes cómo se descubrió el electrón.












No hay comentarios:
Publicar un comentario